Fluoración del agua potable

La fluoración del agua potable —referido a veces como fluorización del agua potable— consiste en la acción controlada de añadir un compuesto fluorado en el agua de abastecimiento público, con el fin de elevar sus niveles de flúor hasta una concentración óptima para prevenir la caries dental. Se considera la concentración óptima de flúor aquella que reduce los niveles de caries, sin que ello provoque una saturación en los tejidos expuestos (fluorosis dental).
Sin embargo, la fluoración del agua presenta controversias por los posibles efectos no deseados sobre la salud, habiendo países que han prohibido esa práctica o que la han dejado de realizar.
No obstante, en aquellos países en los que no se consume agua fluorada, se promueve el consumo de sal o leche fluoradas con el fin de conseguir los mismos efectos sobre la población, si bien en estos casos el consumidor tiene la libertad de elegir si quiere tomar alimentos con flúor o no, mientras que el caso de la fluoración del agua de abastecimiento público, se está obligando al consumidor a tomar un elemento que tal vez no desee tomar.
La OMS recomienda que en cada comunidad se utilice solo un tipo de fluoración sistémica (es decir, del agua, la sal o la leche), combinándola con el uso de dentífricos fluorados, y que se vigile la prevalencia de fluorosis dental para detectar cualquier aumento de la incidencia y evitar que supere los niveles admisibles.
Historia
En 1901, Frederick McKay, dentista en Colorado Springs observó la existencia de una tinción dental permanente en una mayoría de sus pacientes, particularmente en aquellos que habían residido en la zona toda su vida. La coloración era conocida popularmente como "tinción del Colorado", y McKay la rebautizó como "esmalte moteado".
Sospechando un origen relacionado con los abastecimientos de agua, un químico de una compañía que operaba en la zona, H.V. Churchill, se ofreció para hacer análisis de las muestras de agua de su área de trabajo. Se trataba de un acto interesado para descartar que la planta de aluminio para la que él trabajaba pudiera ser responsable de algún vertido nocivo en el agua de la zona que pudiera asociarse al esmalte moteado.
Churchill mandó identificar en las muestras de agua recibidas, todos aquellos elementos aparentemente no significativos e insospechados hasta ese momento en análisis previos. El elemento que atrajo la atención en dichos análisis por su elevada concentración en agua fue el flúor.
A raíz de esto, el Servicio Nacional de Salud Pública encargó la investigación conocida como de las “21 ciudades” sobre la relación entre fluoruros, esmalte moteado y caries dental. Los resultados, conocidos en 1942, llevaron a aconsejar la fluoración del agua de bebida para combatir la caries, en concentraciones comprendidas entre 0,7 y 1,2 ppm. Este rango ha permanecido prácticamente vigente hasta nuestros días, en zonas donde se ha puesto en marcha la fluoración artificial del agua.
En los años 70 empezó a gestarse la idea de que la fluoración podía provocar cáncer. Se hicieron estudios en animales, que arrojaron una relación entre el cáncer de huesos y la ingestión de grandes cantidades de flúor. En los 80 y los 90 se hicieron estudios a gran escala por todo Estados Unidos concluyendo que no había forma de relacionar la ingesta de flúor con algún tipo de cancér, ni se observó ninguna concentración superior de fluoruros en los huesos.
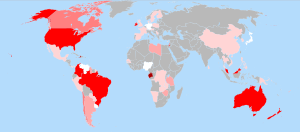
Usos en el mundo
La práctica de la fluorización del agua se realiza de manera muy extendida en los Estados Unidos de América. Se ha introducido también esta práctica en zonas de muchos otros países como por ejemplo en Argentina, Australia, Brasil, Canadá, Chile, Colombia, Corea del Sur, España (principalmente en el País Vasco), Filipinas, Hong Kong, Irlanda, Israel, Malasia, Nueva Zelanda, Singapur, Reino Unido y Vietnam. Se estima que 12 millones de personas en Europa Occidental, 171 millones en EE. UU. (61.5% de la población), y 355 millones a nivel mundial (5.7% de la población mundial) consumen agua fluorizada artificialmente.
Además, a nivel mundial, se estima que al menos 50 millones de personas beben agua fluorada a niveles elevados. El flúor forma parte de la hidroxiapatita que forma parte de los dientes. Es probable que esta cifra sea en realidad mucho más alta. Se usa agua fluorada en muchos países como Argentina, Francia, Gabón, Libia, México, Sri Lanka, Tanzania, Estados Unidos y Zimbabue. En algunos lugares, en particular en partes de Senegal, Sri Lanka, China, y la India, la fluorización del agua sobrepasa los niveles recomendados. Se estima que en China unos 200 millones de habitantes consumen agua fluorada con niveles iguales o superiores a los recomendados. El consumo excesivo de fluoruro puede provocar fluorosis dental y otros síntomas de descalcificación de los huesos como osteoporosis y artritis.[cita requerida]
Controversias por la fluoración del agua
La fluoración del agua presenta muchas controversias, tanto entre los expertos como en la población en general, por diferentes motivos, que van desde la falta de consentimiento del consumidor para tomar una sustancia que algunos califican de innecesaria, hasta los supuestos efectos perjudiciales sobre la salud relacionados con el consumo de flúor.
Los partidarios de la fluoración del agua argumentan que los efectos negativos se producen a partir de consumos elevados y que las dosis aplicadas en el agua son lo suficiente pequeñas como para no afectar a la salud, estando justificado su uso porque los beneficios que obtiene la población por la fluoración son superiores a los riesgos. Las dosis de consumo de flúor recomendadas en EE. UU. y Canadá son de 4mg/día para el hombre, 3mg/día para la mujer y entre 2-3mg/día para niños y adolescentes. Las autoridades sanitarias recomiendan la adición de flúor al agua de consumo, siempre y cuando esta sea deficitaria en el mismo, de modo que su concentración sea como máximo de 1ppm (1mg/litro), cantidad máxima recomendada como saludable. En España, el contenido de flúor (natural o artificial) en las aguas de abastecimiento público suele ser menor a 1ppm.
En algunas localidades se ha interrumpido la fluoración del agua, como por ejemplo en ciudades de Finlandia, Alemania, Japón, Países Bajos, Suecia y Suiza. En ocasiones los objetivos de la fluoración del agua de reducir la incidencia de la caries se pueden conseguir también mediante otras medidas alternativas. Por ejemplo en Francia, Alemania y muchos otros países europeos y no europeos se comercializa sal fluorada y en algunos países también leche enriquecida en flúor. También es muy común utilizar pasta de dientes fluorada o elixires o geles para el lavado de la boca con flúor o barnices para los dientes fluorados.
El flúor y sus compuestos
El flúor es un elemento relativamente abundante en la naturaleza y forma compuestos con la mayoría de los elementos, excepto con los gases nobles helio, argón y neón (que no se combinan con ningún otro elemento, no solo con el flúor). Su nombre fue sugerido a Humphry Davy por A. Ampere en 1812. Sin embargo, fue posible aislarlo a principios del siglo XX, trabajo realizado por Ferdinand Fréderic Henri Moissan, Premio Nobel en 1906. El problema para su aislamiento era que este elemento es el más electronegativo y, por lo tanto, su ion es el más difícil de oxidar.
Una vez aislado, el flúor es un gas diatómico de color amarillo pálido. Es el miembro más liviano de los halógenos. Su masa atómica es 18,998403. Su punto de fusión es 53,54 K y el punto de ebullición es 85,02 K. La energía de ionización del gas es 402 Kcal/mol. Su potencial de reducción estándar es 2,9 V y es el más electronegativo de todos los elementos (4,10 en la escala de Alfred-Rochow, 3,98 en la escala de Pauling, y 3,91 en la escala de Miiliken). El radio covalente es 71 pm y el radio iónico en un ion fluoruro coordinado octaédricamente es 133 pm.
Una vez aislado, el flúor reacciona con las sustancias oxidables, incluso con algunos materiales considerados estables. Es demasiado reactivo para existir en su estado elemental en la naturaleza. Sin embargo, los enlaces que forma con átomos de otros elementos son relativamente fuertes.
Se conocen alrededor de 170 minerales que contienen flúor. Los más abundantes son fluorita (CaF2) y apatita Ca5(PO4)3 (F,OH,CI,1/2CO3) Existen distintos tipos de apatita, dependiendo si el ion unido al fosfato es un fluoruro, cloruro, hidroxilo o carbonato. Este mineral es la principal fuente de fosfatos utilizados como fertilizantes.
Mientras que para los consumidores la utilización de compuestos de flúor en la industria pasa casi inadvertida, algunos compuestos se han vuelto familiares a través de usos menores pero importantes, como aditivos en pastas de dientes y superficies fluoropoliméricas antiadherentes sobre sartenes y hojas de afeitar (teflón por ejemplo).
La hidroxiapatita
La hidroxiapatita, de fórmula Ca5(PO4)3 OH, es un fostato básico de calcio que forma parte de los dientes. Un cristal de hidroxiapatita puede variar su composición mediante un proceso de intercambio iónico. Los iones hidroxilo pueden intercambiarse con iones fluoruro pudiendo modificar, de este modo, un tercio del total de los iones originales. También es posible reemplazar los iones hidroxilo por iones carbonato. El ion calcio puede ser intercambiado con ion magnesio.
Los cristales de hidroxiapatita del esmalte tienen la forma de prismas hexagonales cuyo diámetro es aproximadamente de 0,05 A2. Son más largos que los cristales de hidroxiapatita de la dentina y del cemento. El Streptococcus mutans es el principal microorganismo de la flora bacteriana, cuyas enzimas metabolizan muy rápidamente los hidratos de carbono, en especial la sacarosa.
Este es el nivel crítico que incide en la disolución de los cristales de hidroxiapatita. Se produce la ruptura del esmalte:
- Ca5(PO4)3 OH ---------------- 5Ca+2 + 3PO4-3 + OH-
- 5Ca+2 + 3PO4-3 + 2OH- + 5H4 ---------------- 2Ca+2 + 3CaHPO4. 2H2O
Según la teoría de la quelacion,[cita requerida] el anión lactato se coordina con el calcio formando estructuras queladas.
- 1OF- ---------------- 5CaF2 + 3PO4-3 + OH-
Se puede decir que los iones de lactato tienen la capacidad de solubilizar la apatita de los dientes. Ahora bien, cuando se ingiere fluoruro en concentraciones bajas (1 ppm), la hidroxiapatita se transforma en fluorapatita según la siguiente reacción:
- Ca5(PO4)3OH + F- ----------------- Ca5(PO4)3F + HO
| Control de autoridades |
|
|---|
-
 Datos: Q1125466
Datos: Q1125466
-
 Multimedia: Water fluoridation / Q1125466
Multimedia: Water fluoridation / Q1125466