
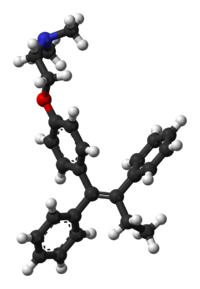
Tamoxifeno
| Tamoxifeno | ||
|---|---|---|

| ||
| ||
| Identificadores | ||
| Número CAS | 10540-29-1 | |
| Código ATC | L02BA01 | |
| PubChem | 2733526 | |
| DrugBank | APRD00123 | |
| ChemSpider | 2015313 | |
| UNII | 094ZI81Y45 | |
| KEGG | D08559 | |
| ChEBI | 41774 | |
| ChEMBL | 83 | |
| Datos químicos | ||
| Fórmula | C26H29NO | |
| Peso mol. |
371.515 g/mol 563.638 g/mol (sal de citrato) |
|
|
O(c1ccc(cc1)/C(c2ccccc2)=C(\c3ccccc3)CC)CCN(C)C
| ||
|
InChI=1S/C26H29NO/c1-4-25(21-11-7-5-8-12-21)26(22-13-9-6-10-14-22)23-15-17-24(18-16-23)28-20-19-27(2)3/h5-18H,4,19-20H2,1-3H3/b26-25-
Key: NKANXQFJJICGDU-QPLCGJKRSA-N | ||
| Datos clínicos | ||
| Vías de adm. | Oral | |
El tamoxifeno es un medicamento que se emplea como terapia complementaria para el cáncer de mama. Se utiliza durante un periodo de 5 años tras finalizar la cirugía y quimioterapia y ha demostrado en diferentes estudios que disminuye considerablemente la probabilidad de que se produzca una reincidencia del tumor.
Se comercializa en forma de comprimidos de 10 y 20 mg. La dosis diaria oscila entre 20 y 40 mg repartidos en una o dos tomas.
Técnicamente se clasifica como modulador selectivo de los receptores estrogénicos. Su mecanismo de acción se basa en su efecto antiestrogénico, es decir bloquea la acción de esta hormona que estimula el desarrollo de las células tumorales. No es útil en todos los cánceres de mama, sino únicamente en aquellos cuyas células presentan receptores específicos para estrógenos. Los tumores de mama son heterogéneos a nivel celular y únicamente el 60% presentan receptores hormonales de este tipo.
Su acción no se limita a la mama, pues diferentes órganos tienen receptores para estrógenos. En el útero tiene paradójicamente un efecto agonista estrogénico y en el hueso mejora la asimilación de calcio, por lo que es beneficioso en la osteoporosis, en el caso de las mujeres menopáusicas. Ya que en las mujeres premenopáusicas puede generar el efecto contrario, aumentado la pérdida de densidad mineral ósea.
En algunas pacientes produce como efecto secundario un aumento en el espesor de la porción más interna del útero (hiperplasia endometrial). En menos del 1% de las personas tratadas puede provocar la aparición de cáncer de útero, por lo que se recomiendan revisiones anuales para detectar esta patología. Otros efectos secundarios son aparición de sofocos y sequedad vaginal.
A pesar de los efectos adversos que a veces son graves, los beneficios del fármaco son muy superiores a sus inconvenientes, mejorando la calidad de vida y la supervivencia de los pacientes.
Toxicidad del tamoxifeno
Hepatitis tóxica por tamoxifeno
Se ha visto en varios estudios que el tamoxifeno puede producir un aumento de las transaminasas (ALAT Y ASAT) en sangre, que son biomarcadores de daño hepático, el daño en los hepatocitos hace que estas enzimas salgan al torrente circulatorio. Se observó también un aumento en el tamaño de los hepatocitos, lo que da lugar a la aparición de colestasis y esteatohepatitis y también se han encontrado casos de ictericia colestásica e hígado graso, pudiendo incluso causar la muerte del paciente.
En los casos publicados predominan dos patrones de lesión: colestasis con o sin citólisis y la esteatohepatitis, patrón de lesión similar al producido por estrógenos.
La conclusión a la que llegamos es que aunque no es muy frecuente la hepatotoxicidad del tamoxifeno, puede producir daño hepático crónico con o sin esteatohepatitis, la mayoría de veces con poca sintomatología clínica, por lo que todas las pacientes en tratamiento con tamoxifeno por periodos prolongados deben tener un control periódico de enzimas hepáticas, como una manera de prevenir las lesiones crónicas.
Toxicidad ocular
Mecanismo de toxicidad
El mecanismo por el cual ejerce la toxicidad ocular el tamoxifeno no se conoce exactamente, pero sabemos que tiene una estructura similar al de otros fármacos de conocida toxicidad ocular como son la imipramina, la amiodarona y la cloroquina, estos al poseer uniones polares y apolares con lípidos que no son metabolizados se acumulan en los complejos intracelulares de los lisosomas.
Primeras evidencias científicas/estudios de la toxicidad del tamoxifeno
La toxicidad ocular secundaria al uso de Tamoxifeno la describió por primera vez en 1978 por Kaiser Kupfer y Lippman ME, que encontraron las siguientes patologías oculares:
- Disminución de la agudeza visual.
- Opacidades corneales
- Opacidades refringentes intrarretinianas
Ashford creía que la toxicidad era totalmente dependiente de la dosis, apareciendo solo a dosis altas, ya que cuando se describió la retinopatía, las pacientes eran tratadas con dosis muy altas de tamoxifeno (del orden de 180 mg/día). Algunos de los signos que se encontraban eran: pequeños depósitos brillantes blanquecinos en la retina interna, alteraciones del epitelio pigmentario y edema de mácula. Las dosis usadas hoy en día son mucho más bajas (10 mg/día) y es raro encontrar formas tan severas, pero aun así se presentan casos con dosis bajas que presentan hemorragias retinianas, alteraciones en el disco óptico y pérdida de la agudeza visual. Por lo tanto podemos decir que la dosis que puede originar retinopatía oscila en un amplio rango y no está claro si la disminución de visión que produce la retinopatía por tamoxifeno es reversible o no.
Zonas de acumulación del tamoxifeno en el globo ocular
- El fármaco se acumula en depósitos subepiteliales, a nivel de la córnea.
- El fármaco se acumula a nivel de la retina, causando maculopatía (retinopatía).
- También está relacionado con la formación de cataratas, debido también a la acumulación a nivel del cristalino.
- La acumulación en el nervio óptico, provoca la aparición de neuritis óptica bilateral seguida de atrofia óptica y pérdida visual.
Cardiotoxicidad
El tamoxifeno puede causar una prolongación del intervalo QT, su mecanismo electrofisiológico consiste en el bloqueo de la corriente rectificadora de potasio. La prolongación del intervalo QT puede dar origen a arritmias (torsades de pointes), siendo el marcador principal para evaluar el riesgo de arritmias asociadas con el consumo de fármacos y que ha llevado a la retirada de distintos agentes antineoplásicos del mercado. No obstante, en la práctica clínica no se registraron incrementos significativos de este intervalo o el aumento del riesgo de arritmias en la población tratada con este fármaco.
| Control de autoridades |
|
|---|