Serpina
| Serpina | ||
|---|---|---|
| Identificadores | ||
| Símbolo | Serpin, SERPIN (root symbol of family) | |
| Pfam | PF00079 | |
| InterPro | IPR000215 | |
| SCOP | 1hle | |
| CDD | cd00172 | |
Estructuras PDB disponibles:
1m37
A:1-378 1hle B:349-379 1jrr A:1-415 1by7 A:1-415 1ova A:1-385 1uhg A:1-385 1jti B:1-385 1att B:77-433 1nq9 L:76-461 1oyh I:76-461 1e03 L:76-461 1e05 I:76-461 1br8 L:76-461 1r1l L:76-461 1lk6 L:76-461 1ant L:76-461 2beh L:76-461 1dzh L:76-461 1ath A:78-461 1tb6 I:76-461 2ant I:76-461p 1dzg I:76-461 1azx L:76-461 1jvq I:76-461 1sr5 A:76-461 1e04 I:76-461 1xqg A:1-375 1xu8 B:1-375 1wz9 B:1-375 1xqj A:1-375 1c8o A:1-300 1m93 A:1-55 1f0c A:1-305 1k9o I:18-392 1sek :18-369 1atu
:45-415
1ezx B:383-415 8api A:43-382 1qmb A:49-376 1iz2 A:43-415 1oo8 A:43-415 1d5s B:378-415 7api A:44-382 1qlp A:43-415 1oph A:43-415 1kct :44-415 2d26
:47-415 1hp7
A:43-415 3caa A:50-383 1qmn A:43-420 4caa B:390-420 2ach A:47-383 1as4 A:48-383 1yxa B:42-417 1lq8 F:376-406 2pai B:374-406 1pai B:374-406 1jmo A:119-496 1jmj A:119-496 1oc0 A:25-402 1dvn A:25-402 1b3k D:25-402 1dvm D:25-402 1a7c A:25-402 1c5g A:25-402 1db2 B:26-402 9pai A:25-402 1lj5 A:25-402 1m6q A:138-498 1jjo D:101-361 1imv A:49-415 | ||
Las serpinas (del inglés, serine protease inhibitors) son una superfamilia de proteínas caracterizadas principalmente por ser inhibidores de proteasa, ampliamente distribuida en los seres vivos ya que se pueden encontrar en todos los eucariotas y en algunos procariotas. Si bien la mayoría de las serpinas tienen la función de inhibir serina proteasas, otras inhiben caspasas, y cisteína proteasas como la papaína. También se encuentran serpinas con otras funciones tales como el transporte de hormonas, chaperonas moleculares o la supresión de tumores.
Las serpinas regulan tanto los procesos de formación de coágulos (trombosis) como los de la disolución de ellos (trombólisis), la respuesta inmune, la reparación del tejido conectivo, la apoptosis, el transporte de hormonas, la unión de corticosteroides, la función neuronal y la presión sanguínea.
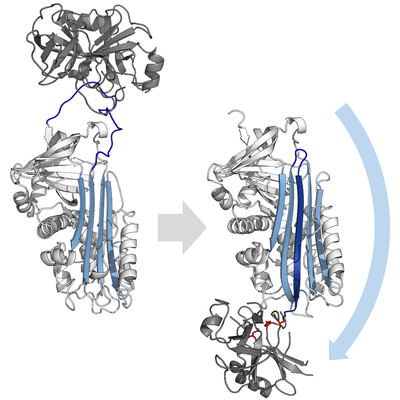
Las serpinas son «inhibidores suicidas» que actúan como carnada para sus serina proteasas objetivos. Este inusual mecanismo de acción consiste en inhibir la proteasa de manera irreversible, puesto que al unirse ambas moléculas son sometidas a un gran cambio conformacional que altera sus sitios activos quedando inactivas en forma permanente.
Consecuentemente estas proteínas son el objetivo de investigación médica, ya que su cambio conformacional único las vuelve de alto interés biológico estructural y de investigación a cerca del doblaje de proteínas.
El mecanismo de cambio conformacional contiene ciertas ventajas, pero también algunas desventajas. Por un lado, las serpinas son vulnerables a mutaciones que pueden resultar en serpinopatías como el doblaje erróneo de las proteínas y la formación de polímeros inactivos de cadenas largas. La polimerización de serpinas no solo reduce la cantidad de inhibidores activos sino que también conlleva la acumulación de los polímeros, causando muerte celular y falla de órganos .
Aunque la mayoría de las serpinas controlan las cascadas proteolíticas, algunas proteínas con estructura de serpina no son inhibidores de enzimas, pero realizan diversas funciones como almacenamiento (como en el huevo blanco—ovoalbúmina), transporte como en las proteínas de transporte de hormonas (Globulina fijadora de tiroxina, globulina fijadora de cortisol) y de proteína chaperona(HSP47). El término serpina se usa para describir a estos miembro también, a pesar de su función no inhibitoria ya que están relacionados evolutivamente.
Historia
El acrónimo serpina fue establecido porque las primeras serpinas en ser identificadas actuaban como quimotripsina serina proteasa.
La actividad inhibidora de la proteasa en el plasma de la sangre se reportó por primera vez a finales de 1800, hasta los 50 que las serpinas antitrombina y alfa 1-antitripsina fueron aisladas. la investigación inicial se concentraba en el papel sobre la enfermedad humana: deficiencia de alfa 1-antitripsina que es uno de los desórdenes genéticos más comunes, causa enfisema, y la deficiencia de antitrombina resulta en trombosis.
En la década de los 80, se volvió claro que estos inhibidores eran parte de una superfamilia de proteínas relacionadas entre sí que incluían inhibidores de proteasa (alfa 1-antitrpsina) y no inhibidores (ovalbúlima). Durante el mismo periodo de tiempo, las primeras estructuras de la serpina fueron estudiadas (primero en su conformación relajada y después en la estresada). La estructuras indicaba que el mecanismo inhibidor involucraba un cambio conformacional inusual y promovía el siguiente punto de enfoque estructural en los estudios de la serpina.
Hasta ahora han sido identificadas más de 1000 serpinas incluyendo, 36 proteínas humanas, además de moléculas en todos los reinos. En los 2000, una nomenclatura sistemática fue introducida para categorizar miembros de la superfamilia de serpinas basado en sus relaciones evolutivas. Las serpinas son, por lo tanto, la superfamilia más grande y diversa de inhibidores de proteasa.
Clasificación
Las serpinas constituyen la familia de inhibidores de proteasas más numerosa y diversa. Se han identificado alrededor de 1500 serpinas en todos los reinos, incluyendo las 36 serpinas humanas. Las serpinas se han clasificado en clados de acuerdo a las similitudes en sus secuencias. Los clados se clasifican de la A a la P, de los cuales los 9 clados de la A a la I representan las serpinas humanas. El gen que los codifica se ha denominado SERPIN, y para efectos de la clasificación de la serina específica, la letra del clado se anota a continuación y finalmente se le agrega el número del gen, por ejemplo, para la alfa 1-antitripsina la identificación es SERPINA1 (serpina del clado A, gen 1).
Distribución
Humanos
El genoma humano codifica 9 clados de serpinas, que van desde el clado A (SERPINA) hasta el clado I (SERPINI), incluyendo 29 proteínas de serpina inhibitorias y 7 no inhibitorias.
El sistema usado para nombrar las serpinas humanas está basado en un análisis filogenético de aproximadamente 500 serpinas del 2001, con proteínas llamada serpin XY, donde X es el clado de proteína y Y el número de proteínas dentro de ese clado. Las funciones de las serpinas humanas han sido determinadas por una combinación de estudios bioquímicos, desórdenes humanos genéticos, y modelos de ratones knockout T.
| Tabla de serpinas humanas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Otros mamíferos
Muchas serpinas de mamíferos han sido identificadas demostrando no tener una ortología obvia que compartir con la contraparte humana de la serpina. Ejemplos incluyen numeroras serpinas de roedores (particularmente algunas de las serpinas de murino intraelular) como también las serpinas uterinas. El término serpina uterina se refiere a los miembros del clado A de serpinas que son codificadas por el gen SERPINA14. Las serpinas uterinas son producidas por el endometrio en un grupo restringido de mamíferos bajo la influencia de progesterona y estrógeno. Probablemente son inhibidores de proteinasa no funcionales y pueden funcionar durante el embarazo para inhibir la respuesta inmune materna contra el zigoto o para participar en el transporte transplacentaria.
Insectos
El genoma de Drosophila melanogaster contiene 29 genes codificadores de serpina. El análisis de la secuencia de aminoácidos ha colocado 14 de estas serpinas en el clado de serpinas Q y 3 serpinas en el clado K con las 12 restantes clasificadas como serpinas huérfanas al no pertenecer a ningún clado. El sistema de clasificación de clados es difícil de usar para Drosophila serpins y en lugar, un sistema de nomenclatura se adoptó basado en la posición de los genes de serpina en los cromosomas de Drosophila. Trece de las serpinas de Drosophila se encuentran como genes aislados en el genoma (incluyendo Serpina-27A,), con las 16 restantes organizadas en 5 agrupaciones de genes que ocurren en las posiciones del cromosoma 28D (2 serpinas), 42D (5 serpinas), 43A (4 serpinas), 77B (3 serpinas) y 88E (2 serpinas).
Estudios en las serpinas de Drosophila revelan que la Serpina-27A inhibe la proteasa de pascua(la proteasa final en el Nudel) Al igual que su rol central en los patrones embriónicos, la señalización también es importante para la respuesta inmune innata en insectos. Aparentemente, la serpina-27A también funciona para controlar la respuesta inmune de los insectos.
Nemátodos
El genoma del gusano nematodo C. elegans contiene 9 serpinas, de las que ninguna tiene secuencias de señalización y por lo tanto son intracelulares. Sin embargo, solo 5 de estas serpinas parecen funcionas como inhibidores de proteasa. Un, SRP-6, realiza una función protectora y protege contra la ruptura inducida por estrés asociada con calpaína. Además, SRP-6 inhibe las proteasas de cisteían lisosomales liberadas por la ruptura del lisosoma.
Plantas
Las serpinas de las plantas estaban entre los primeros miembros de la superfamilia en ser identificados. Las serpinas de plantas son poderosos inhibidores de proteasas de serina como quimotripsina de mamíferos, in vitro, el ejemplo mejor estudiado siendo la serpina Zx (BSZx), que es capaz de inhibir tripsina y quimotripsina al igual que a diversos factores de coagulación. Sin embargo, parientes cercanos de la proteasa de serina como quimotripsina están ausentes en plantas. El RCL de varias serpinas de grano de trigo y centeno contiene secuencias que repiten poli-Q similares a esas presentes en las proteínas de almacenamiento de prolamina del endoesperma. Ha sido entonces sugerido que las serpinas de las plantas funcionen mejor en inhibir proteasas de insectos o microbios que de otra manera digerirían las proteínas de almacenamiento de granos. Soportando esta hipótesis diferentes serpinas de plantas han sido identificadas en la savia del floema de la calabaza (CmPS-1) y plantas de pepino. Aunque se observó una correlación inversa entre la expresión de CmPS-1 y la supervivencia áfida, in vitro más experimentación reveló que el CmPS-1 recombinante no parecía afectar la supervivencia de los insectos.
Roles alternativos y las proteasas objetivo para las serpinas de las plantas han sido propuestos. La serpina Arabidopsis, AtSerpin1 (At1g47710; 3LE2 ), regula el punto de control sobre la muerte celular programada al marcar como objetivo (RD21) la proteasa de cisteína como papaína. Otras dos serpinas Arabidopsis , AtSRP2 (At2g14540) y AtSRP3 (At1g64030) parecen estar relacionadas con respuestas al daño del ADN.
Hongos
Una sola serpina fungal ha sido caracterizada: celpina de Piromyces spp. cepa E2. Piromyces es géneroode hongo anaeróbico encontrado en el intestino de los rumiantes y es importante para la digestión de plantas. Se predice que la celpina es inhibitoria y contiene dos dominion con terminales-N además del dominio de la serpina. se sugiere que la celpina pueda proteger la celulosoma de proteasas de plantas.
Procariotas
Genes predichos de serpina están distribuidos esporádicamente en procariotas. Estudios In vitro de algunas de las moléculas han revelado que son capaces de inhibir proteasas, y se sugiere que funcionan como inhibidores in vivo. Varias serpinas procariotas se encuentran en extremofilos. En contraste con las serpinas de mamíferos, estas moléculas poseen gran resistencia a la desnaturalización por calor. El papel preciso de la mayoría de las serpinas bacterianas permanece sin conocerse, aunque la serpina de Clostridium thermocellum se localiza en la celulosoma. Se considera que el rol de las serpinas asociadas a la celulosoma puedan ser de prevención de la actividad de proteasas no deseadas contra la celulosoma.
Viral
Las serpinas también se expresan en virus como una manera de evitar la defensas inmunes del huésped. En particular, las serpinas se expresan por virus de viruela, incluyendo viruela de la vaca (vaccinia) y viruela del conejo (myxoma), son de interés porque su uso potencial como nueva terapia para desórdenes inmunes e inflamatorios como para terapia de trasplante. Serp1 suprime la respuesta inmune innata de TLR y permite la supervivencia del injerto cardiaco en ratas. Crma y Serp2 son ambos inhibidores de clases cruzadas y tienen como objetivo tanto proteasas de serina como de cisteína. En comparación con su contraparte en mamíferos, las serpinas virales contienen deleciones significativas de elementos de estructura secundaria. Específicamente, el crmA carece de la hélice-D en la misma proporción que las hélices A y E.
Estructura
La serpina, en su forma nativa o activa, es una molécula monomérica compuesta por una secuencia de 330 a 550 aminoácidos con una estructura secundaria de hélices y láminas. En la práctica esta molécula puede encontrarse en diferentes estados: activa, latente, dividida, delta y polimérica.
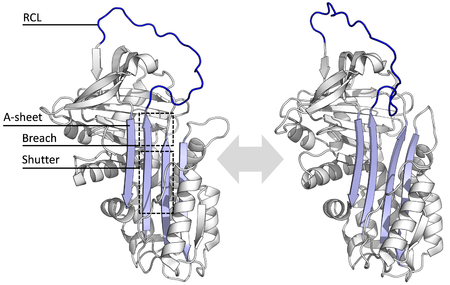
Las diferentes serpinas comparten similitudes en su secuencia que varían entre un 17 a un 95%, sin embargo, su estructura posee secuencias clave comunes que permiten una conformación estable que típicamente está compuesta por tres láminas beta plegadas (denominadas A, B y C) y ocho o nueve hélices alfa (denominadas hA a hI) y un ciclo central reactivo (RCL, por el inglés reactive center loop).
Las regiones más significantes para la función de la serpina son la plegada-A y su loop de centro reactivo(RCL). La plegada-a incluye dos hebras-β que están en orientación paralela con una región entre ellas llamada 'shutter', y una región arriba llamada 'brecha'. El RCL forma la interacción inicial con la proteasa como objetivo en moléculas inhibidoras. Se han descifrado estructuras mostrando el RCL ya sea totalmente expuesto o parcialmente insertado en la plegada-A, y se piensa que las serpinas están en equilibrio dinámico entre estos dos estados. El RCL también hace interacciones temporales con el resto de la estructura y es por lo tanto sumamente flexible y es expuesto al solvente.
Las estructuras de serpinas que han sido determinadas, cubren varios tipos diferentes de conformaciones, que han sido necesarias para el entendimiento de su mecanismo de acción de múltiples pasos. La biología estructural ha jugado un papel centrar en el entendimiento de la función y biología de las serpinas.
Función biológica y ubicación
Funciones
La mayoría de las serpinas controlan por inhibición cascadas proteolíticas catalizadas por enzimas proteasas de la familia de las quimotripsinas, mientras que otras no son inhibitorias de otras enzimas sino que realizan funciones variadas, tales como almacenamiento (es el caso de la ovoalbumina), proteínas de transporte hormonal (globulina fijadora de tiroxina, globulina fijadora de cortisol), genes supresores tumorales (como la maspina), regulación de la tensión arterial y desarrollo de linfocitos B, entre muchas otras. Se emplea el término serpina para este tipo de enzimas no inhibitorias, a pesar de su contradictoria función.
Inhibición de la proteasa
La mayoría de las serpinas son inhibidores de proteasa, siendo su objetivo las proteasas de serina como quimotripsina. Estas proteasas poseen un residuo de una serina nucleofílicaMen una tríada catalítica. Algunos ejemplos, incluyen trombina, tripsina y las elastas de neutrófilos humanos. Las serpinas actúan como inhibidores irreversibles y suicidas al atrapar un intermediario del mecanismo catalítico de la proteasa.
Algunas serpinas inhiben otra clase de proteasas, normalmente proteasas de cisteína y se le conoce como inhibidores de clase cruzada. Estas enzimas difieren de la serinaproteasas en que una cisteína nucleofílica en lugar de una serina en su sitio activo. No obstante, la química enzimática es la misma para las dos clases de proteasa. Ejemplos de serpinas inhibidoras de clase cruzada incluyen la serpina B4, un antigen 1 de carcinomas de células escamosas(SCCA-1) y la serpina aviar, una proteína de etapa específica, mieloide y eritoride de terminación nuclear.
Aproximadamente dos tercios de las serpinas humanas realizan roles extracelulares, inhibiendo proteasas en el flujo sanguíneo para modular sus actividades. Por ejemplo las serpinas extracelulares regulan las cascadas proteicas esenciales para la coagulación de la sangre (antitrombina), las respuestas inmune e inflamatoria (antitripsina, antiquimotripsina y el inhibidor C1) y remodelación de tejido (PAI-1). Al inhibir las proteasas de señalización de cascada, solo pueden afectar el desarrollo. La tabla de serpinas humanas encontrado al final del documento proporciona ejemplos del rango de funciones realizadas por las serpinas humanas al igual que algunas de las enfermedades que resultan de la deficiencia de serpinas.
Las proteasas, objetivo de las serpinas inhibiidoras intracelulares han sido difíciles de identificar debido a que varias de estas moléculas parecen realizar tareas que se superponen. Además muchas serpinas humanas carecen de los equivalentes funcionales precisos en organismos modelos como el ratón. Sin embargo, una función importante de las serpinas intracelulares puede ser proteger de la actividad inapropiada de las proteasas dentro de la célula. Por ejemplo, uno de las serpinas mejor caracterizadas es la serpina B9, que inhibe la proteasa de gránulo citotóxico, granzima B. Al hacerlo, la serpina B9 puede proteger contra la liberación inadvertida de granzima B y la activación prematura o no deseada de los mecanismos de muerte celular.
Algunos virus usan serpinas para interrumpir las funciones de las proteasas en su huésped. La serpina viral de la viruela de las vacas CrmA se usa para evitar respuestas inflamatorias y apoptóticas de las células huéspedes infectadas. La CrmA aumenta la infección al suprimir la respuesta inflamatoria del huésped a través de la inhibición de IL-1 y el procesamiento de L-18 por la proteasa de cisteína caspasa-1 . En eucariontes una serpina de planta inhibe metacaspasas y una proteasa de cisteína como papaína
Roles no inhibitorios
Las serpinas extracelulares no inhibitorias también realizan un gran conjunto de roles importantes La globulina fijadora de tiroxina y la transcortina transportan las hormonas tiroxina y cortisol respectivamente. La serpina de ovalbúlmina, no inhibitoria es la proteína más abundante del huevo blanco. Su función exacta no se conoce, pero se cree que es una proteína de almacenamiento para fetos en desarrollo. La serpina de choque térmico 47 es una chaperona, esencial para del doblaje apropiado del colágeno. Actúa estabilizando la triple hélice del colágeno mientras está siendo procesada en el retículo endoplasmático.
Algunas serpinas son tanto inhibidoras de proteasas y realizan otras tareas. Por ejemplo, el inhibidor nuclear de proteasas de cisteina MENT, en pájaros también actúa como una molécula remodeladora de cromatina en las células rojas de un ave.
Cambio conformacional y mecanismo inhibitorio
Las serpinas inhibitorias no inhiben a su objetivo, las proteasas por su típico mecanismo competitivo (candado y llave) usado por la mayoría de los inhibidores de proteasa pequeños ( Kunitz-type inhibitors). En lugar de eso, las serpinas usan un cambio conformacional inusual, el cual altera la estructura de la proteasa y previene que complete la catálisis. El cambio conformacional incluye que el RCL se mueva al extremo contrario de la proteína e insertando una β-plegada A, formando una hebra-β extra antiparalela. Esto convierte a la serpina de un estado estresado a un estado relajado de baja energía(transición de S a R).
La serpina y las proteasas de cisteína catalizan el rompimiento de un enlace peptídico por un proceso de dos pasos. Inicialmente, los residuos catalíticos del sitio activo de la tríada realiza un ataque nucleofílico en el enlace peptídico del sustrato, esto libera las nuevas terminales-N y forma un enlace de éster covalente entre la enzima y el sustrato. Este complejo covalente entre la enzima y el sustrato se llama un intermediario acil-enzima. Para sustratos estándares, el puente de éster es hidrolizado y una nueva terminal-C se libera para completar la catálisis. Sin embargo, cuando una serpina es separada por una proteasa, rápidamente atraviesa una transición de S a R antes de que el intermediario acil-enzima sea hidrolizado. La eficiencia de la inhibición depende del hecho que la velocidad cinética relativa del cambio conformacional sea varios órdenes de magnitud más rápida que la hidrólisis de la proteasa.
Ya que el RCL está atado todavía covalentemente a la proteasa por el enlace de éster, la transición de S a R, toma a la proteasa de la cima al fondo de la serpina y distorsiona la tríada catalítica. La proteasa distorsionada solo puede hidrolizar el intermediarios acil-anzima extremadamente despacio, y entonces la proteasa permanece covalentemente unida desde días hasta semanas. Las serpinas se clasifican como inhibidores irreversibles y como inhibidores suicidas ya que cada proteína de serpina inactiva permanentemente una sola proteasa y solo puede funcionar una vez.
Activación alostérica

La movilidad conformacional de las serpinas proporciona una ventaja clave sobre los inhibidores de proteasa de candado y llave. En particular, la función de serpinas inhibitorias puede ser regulada por interacciones alostéricas con los factores específicos. Las estructuras cristalinas en rayos X de la antitrombina, el cofacto heparina II, MENT y la antiquimotripsina revelan que estas serpinas adoptan una conformación cuando en los primeros dos aminoácidos del RCL, están insertadas las β-plegadas A. La conformación parcialmente insertada es importante porque los cofactores pueden cambiar conformacionalmente ciertas serpinas insertadas parcialmente en una forma completamente expulsada. Este arreglo confromacional hace a la serpina un inhibidor más eficiente.
El ejemplo arquetípico de esta situación es la antitrombina, que circula en el plasma en un estado relativamente inactivo al estar parcialmente insertado. Un ejemplo de esta situación es la antitrombina, que circula en el plasma en un estado parcialmente inactivo parcialmente inactivo. Lo primero que se determina es que el residuo (de arginina P1) apunta hacia el cuerpo de la serpina y no está disponible para la proteasa. Después de unirse, una secuencia de pentasacáridos de gran afinidad en una cadena larga de heparina, la antitrombina sufre un cambio conformacional, la expulsión del RCL, y la exposición de la arginina P1. La heparina de pentasacáridos de antitrombina es, entonces un inhibidor más eficiente de la trombina y factor Xa. Además, las proteasas de coagulación también contienen sitio de unión (llamados exositios) para la heparina. La heparina, por lo tanto, también actúa como un templados para la unión de ambas, la proteasa y la serpina, acelerando dramáticamente la interacción entre las dos entidades. Después de la interacción inicial, el complejo final de la serpina se forma y la mitad de la heparina se libera. Esta interacción es fisiológicamente importante. Por ejemplo después de una herida a la pared de los vasos sanguíneos, la heparina es expuesta y la antitrombina se activa para controlar la respuesta de coagulación. Entender la base molecular de esta interacción permite el desarrollo de Fondaparinux, una forma sintética de heparina pentasacárida usada como un fármaco anticoagulante.
Conformación latente

Ciertas serpinas son sometidas espontáneamente a la transición de S a R sin haber sido cortadas por una proteasa, para formar una conformación denominada como el estado latente. Las serpinas latentes son incapaces de interactuar con proteasas y por lo tanto ya no son inhibidores de proteasa. El cambio conformacional a estado latente no es exactamente lo mismo que la transición de S a R de una serpina cortada. Ya que el RCL, sigue intacto, la primera hebra de la plegada-C tiene que despegarse para permitir la inserción completa del RCL.
La regulación de la transición a estado latente puede actuar como un mecanismo de control en algunas serpinas como en PAI-1. Aunque PAI-1 se produce en la conformación inhibitoria S, se auto.inactiva aal cambiar a estado latente, a menos que se una al cofactor vitronectina. De manera similar, la antitrombina puede convertirse espontáneamente a su estado latente, como un mecanismo de modulación adicional a su activación alostérica con heparina. Finalmente, la terminal-N, una serpina de Thermoanaerobacter tengcongensis, se necesita para asegurar la molécula en su estado nativo inhibitorio. La ruptura de las interacciones hechas por la región de la terminal N resultan es cambios conformacionales espontáneos de la serpina a su conformación latente. .
Cambio conformacional en funciones no inhibitorias
Algunas serpinas no inhibitorias también usan el cambio conformacional de la serpina como parte de su función. Por ejemplo, la forma nativa (S) de la globulina fijadora de tiroxina tiene una gran afinidad por la tiroxina, mientras que la forma cortada (R) tiene poca afinidad . De manera similar, la transcortina tiene mayor afinidad por el cortisol cuando está en su estado nativo (S) que cuando está en su estado cortado (R). Entonces, en estas serpinas, el RCL cortado y la transición de S a R se requiere para permitir la liberación de ligandos en lugar de la inhibición de proteasas.
En algunas serpinas, la transición de S a R puede activar eventos de señalización celular. En estos caso, una serpina que ha formado un complejo con su proteasa objetivo, es reconocida por un receptor. El evento de unión entonces conduce a una disminución de señalización por el receptor. La transición de S a R es usada para alertar células de la presencia de actividad de proteasa. Esto difiere de su mecanismo usual donde, las serpinas afectan la señalización simplemente al inhibir proteasas implicadas en una cascada de señalización.
Degradación
Cuando una serpina inhibe una proteasa, forma un complejo permanente que necesita ser eliminado. Para las serpinas extracelulares, los complejos finales de serpina-enzima son rápidamente limpiados de la circulación. Un mecanismo por el que esto ocurre en mamíferos es a través de la proteína relacionada con el receptor de lipoproteínas de baja densidad (LRP) que se une a complejos inhibitorios hechos por la antitrombina, PA1-1, y la neuroserpina, provocando captación celular. De manera similar, la serpina de Drosophila se degrada en el lisosoma después de haber sido llevada dentro de la célula por el recpeto Lipoforina 1 (homólogo al recepeto LDL de la familia de mamíferos.
Enfermedad y serpinopatías
Las serpinas son parte de un gran arreglo de funciones fisiológicas, y por lo tanto, las mutaciones en los genes codificándolas pueden causar una serie de enfermedades. Mutaciones que cambian la actividad, la especificidad o propiedades agregadas de las serpinas pueden afectar la manera en que funcionan. La mayoría de las enfermedades relacionadas con las serpinas son el resultado de una polimerización de serpinas en conjuntos, aunque otro tipo de mutaciones ligadas a enfermedades pueden ocurrir. El desorden de la deficiencia de α-Antitripsina es una de las enfermedades hereditarias más comunes.
Inactividad o ausencia
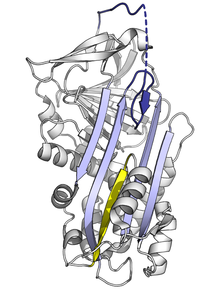
Ya que el doblaje de la serpina estresada es de energía alta, las mutaciones pueden causar que se cambien incorrectamente a conformaciones de baja energía(relajadas o latentes) antes de que realicen correctamente su función inhibitoria.
Las mutaciones que afectan la velocidad o que tanto se inserta el RCL en la plegada-A puede causar que la serpina sufra su cambio conformacional de S a R antes de haber interactuado con una proteasa. Como una serpina solo puede hacer este cambio conformacional una sola vez, la serpina ahora es inactiva e incapaz de controlar apropiadamente a la proteasa. De igual manera, las mutaciones que promueven la transición inapropiada hacia el monomérico estado latente causan enfermedades al reducir la cantidad de serpina inhibitoria. Por ejemplo, ambas variantes enfermas de antitrombina wibble y wobble, promueven la formación del estado latente.
La estructura de la antiquimotripsina enferma (L55P) reveló otra, "la conformación- δ" inactiva. En la conformación- δ, se insertan cuatro residuos del RCL en la parte superior de la β-plegada A. La mitad del fondo de la plegada se llena como resultado de una de las α-hélices (hélice F) cambiando parcialmente a una conformación de hebra-β, completando la unión de hidrógeno de la β-plegada. No está claro si otras serpinas pueden adoptar este confórmero y si esta conformación tiene un tarea funcional, pero se especula que la conformación-δ puede ser adoptada por la globulina fijadora de tiroxina durante la liberación de tiroxinas. Las proteínas no inhibitorias relacionadas con las serpinas también pueden causar enfermedades cuando mutan. Por ejemplo la mutaciones en SERPINF1 causan osteogenesis imperfecta tipo VI en humanos.
En la ausencia de la serpina requerida, la proteasa que normalmente regularía está hiperactiva, conduciendo a patologías. Consecuentemente, una simple deficiencia de serpinas (una mutación nula) puede resultar en enfermedad.
Cambio de especificidad
En algunos casos raros, un solo cambio en los aminoácidos del RCL de la serpina altera su especificidad y ataca a la proteasa incorrecta. Por ejemplo la mutación de Antitripsina-Pittsburgh (M358R) causa que la serpina α1-antitrypsin inhiba a la trombina causando un desorden de hemorragia.
Polimerización y acumulación
La mayoría de las enfermedades de serpinas se deben a la acumulación de proteínas y se denominan como "serpinopatías". Las serpinas son vulnerables a mutaciones que causen enfermedades que promueven la formación de polímeros mal doblados debido a sus estructuras inestables. Serpinpatías bien caracterizadas incluyen la deficiencia de α1-antitropsina, que puede causar enfisema familiial y en algunos casos cirrosis, ciertas formas familiales de trombosis relacionadas con la deficiencia de antritrombina,
Cada monómero del acumulado de serpinas existe es su conformación inactiva, relajada (con el RCL insertado en la plegada-A). Los polímeros son, por lo tanto, hiperestables a temperatura e incapaces de inhibir proteasas. Las serpinopatías entonces causan patologías similares a otra protepatías (enfermedades de prion) a través de dos mecanismos. Primero, la ausencia de serpinas activas resulta en la actividad incontrolable de las proteasas y la destrucción de tejidos. Segundo, los polímeros hiperestables obstruyen el retículo endoplasmático de las células que sintetizan las serpinas, eventualmente resultando en muerte celular y daño de tejidos. En el caso de la deficiencia de antitripsina, los polímeros de antitripsina provocan la muerte de células hepáticas y cirrosis. Dentro de la célula, los polímeros de serpina se remueven lentamente por degradación en el retículo endoplasmático. Sin embargo, los detalles de como los polímeros de serpina causan la muerte celular todavía no se entiende completamente.
Se cree que los polímeros fisiológicos de serpina se forman a través de un cambio de dominio, donde un segmento de una proteína de serpina se inserta en otro. Los cambios de dominio ocurren cuando las mutaciones o los factores ambientales interfieren con las etapas finales del doblaje de la serpina, haciendo que los intermediarios de alta energía se doblen mal. Tanto las estructuras de los dímeros como de los trímeros que sufrieron cambio de dominio han sido resueltas. En el dímero (de antitrombina), el RCL y parte de la plegada-A se incorporan en la plegada-A de otra molécula de serpina. el trímero de dominio cambiado (de antitripsina) forma, a través del intercambio de una región completamente diferente de la estructura, la beta-plegada (con el RCL de cada molécula insertado en su propia plegada-A). También se ha propuesto que las serpinas puedan formar cambios de dominio al insertar el RCL de una proteína en la plegada-A de otra (polimerización de plegada-A). Estas estructuras de dímeros y trímeros con cambio de dominio son suficientemente fuertes para ser los componentes de los acumulados de polímeros causantes de enfermedades, pero el mecanismo todavía no es claro.
Estrategias terapéuticas
Varios acercamientos terapéuticos están siendo investigados para tratar la serinpatía más común, la deficiencia de antitripsina. La terapia de aumento de antitripsina es aprobada para la deficiencia severa de antitripsina, relacionada con enfisema pulmonar. En esta terpia, la antitripsina es pruificada del plasma de donadores de sangre y administrada por intravenosa (Prolastin). Para tratar la deficiencia severa de antitripsina, el trasplante de pulmones e hígado ha sido efectivo. En modelos animales el direccionamiento de genes en células madre pluripotentes inducidas ha sido exitosamente usado para corregir el defecto de polimerización de antitripsina y para restaurar la habilidad del hígado mamífero de secretar antitripsina activa. Pequeñas moléculas también han sido diseñadas que bloquean la polimerización de antitripsina in vitro.
Evolución
Las serpinas son la superfamilia de proteínas inhibidoras más grande y más distribuida. Se pensaba que estaban restringidas a organismos eucariotes. pero desde entonces, han sido encontradas en bacteria, arquea y algunos virus. Permanece incierto si los genes procariotes son descendientes de una serpina procariótica ancestral o el producto de una transferencia genética horizontal de eucariontes. La mayoría de las serpinas permanecen a un clado filogenético, si vienen de plantas o animales, indicando que las serpinas intracelulares y extracelulares pueden haberse separado antes de las plantas y los animales. Excepciones incluyen la serpina de choque intracelular de calor HSP47, que es una chaperon esencial para el doblaje apropiado del colágeno y ciclos entre cis-Golgi y el retículo endoplasmático.
La inhibición de proteasa es considerada la función ancestral, con miembros no inhibidores resultado de neofuncionamiento evolucionario de la estructura. El cambio conformacional de S a R también ha sido aaptado por algunas serpinas que se unen para regular la afinidad por sus objetivos.
Investigaciones
Como las serpinas controlan procesos celulares tales como la coagulación y la inflamación, son proteínas blanco para investigaciones científicas. Las serpinas también tienen importancia para la genómica estructural y el estudio del plegamiento de proteínas debido a que son capaces de dramáticos y muy únicos cambios en sus estructuras en el proceso de la inhibición enzimática. Esa característica es poco usual, ya que los inhibidores de las proteasas tienden a fusionarse con la sencillez de una llave y su cerradura, con formas moleculares precisas en el sitio activo de la enzima. La desventaja de los mecanismos conformacionales de las serpinas es que las hace susceptibles a mutaciones que causan polímeros de larga cadena que son inactivas.
Véase también
-
 Datos: Q420068
Datos: Q420068
-
 Multimedia: Serine protease inhibitors / Q420068
Multimedia: Serine protease inhibitors / Q420068